Схемотехника: Знаем ли мы, что такое АНОД? и что такое КАТОД?

Данная статья родилась как разбор статьи: «Б.Г.Хасапова — Знаем ли мы, что такое АНОД?»
«Автор статьи больше всего боится, что неискушённый читатель далее заголовка читать не станет. Многие считают, что определение терминов анод и катод известно каждому грамотному человеку… Но не так много можно найти вещей страшнее полузнания. (примечание: это и называется „ложью“ — поверхностные и искажённые знания) Ошибкам в применении терминов АНОД и КАТОД нет числа. »
В электронике
«Катод – отрицательный электрод, анод – положительный»? Нет, ложь!
«ГОСТ 15596-82. ИСТОЧНИКИ ТОКА ХИМИЧЕСКИЕ. Термины и определения» на странице 3 даёт точное определение: «Отрицательный электрод химического источника тока это электрод, который при разряде источника является анодом» [через него в источник электрический ток входит из внешней цепи].
То же самое, «Положительный электрод химического источника тока это электрод, который при разряде источника является катодом» [через него из источника электрический ток выходит во внешнюю цепь]. 
Сами термины ввёл М.Фарадей (в январе 1834г., «во избежание неясности и неопределенности, а также ради большей точности»): «Поверхности, у которых электрический ток входит в вещество и из него выходит, являются весьма важными местами действия и их необходимо отличать от полюсов… Если бы электрический ток шел вдоль экватора по направлению кажущегося движения солнца: назвать ту поверхность, которая направлена на восток – анодом, а ту, которая направлена на запад – катодом.» Примерное толкование: «анод – ВОСХОД, путь солнца вверх — ток входит», «катод – ЗАХОД, путь солнца вниз — ток выходит»… С направлением тока эти термины связаны весьма опосредованно, поэтому запоминать лучше ГОСТовское определение или следующие:
В радиолампе/диоде (потребителе электроэнергии) в ПРЯМОМ ВКЛЮЧЕНИИ («в открытом состоянии»): в Анод — [из внешней цепи, в элемент] входит электрический ток. (Не путать с направлением электронов!) Катод — соответственно, электрод из которого выходит электрический ток [во внешнюю цепь, из элемента]. 
Однако, замечание: При ОБРАТНОМ ВКЛЮЧЕНИИ (когда «вентиль закрывается») — полупроводниковые диоды практически не проводят электрический ток («обратный пробой» не считаем), а электровакуумные диоды (радиолампы, кенотроны) вообще не проводят обратный ток. В виду этого, условно принято считать, что обратный ток через диоды не идёт. (Но в этом случае, у выводов диода [формально] отсутствуют функции «катод» и «анод»!)
Поэтому для ясности решили: у диодных элементов (в отличие от аккумуляторов) названия выводов «катод» и «анод» — не меняются от схемы включения, и жёстко привязаны к физическим выводам (электродам) прибора, в зависимости от внутреннего строения прибора (в полупроводниковых диодах — в привязке к типам проводимости кристаллов; в электронных лампах — в привязке к электроду эмитирующему электроны, где находится нить накала).
Впрочем, через полупроводниковые приборы (разновидности диода) «стабилитрон» и «супрессор» — обратный ток даже течёт «немножко», но это уже другая история, не меняющая существующего порядка наименований и определений. 
Как заметил TheLongRunSmoke : «В случае с кенотроном, включив его в обратном направлении — физический смысл электродов изменится, но наименование электродов не изменится.»

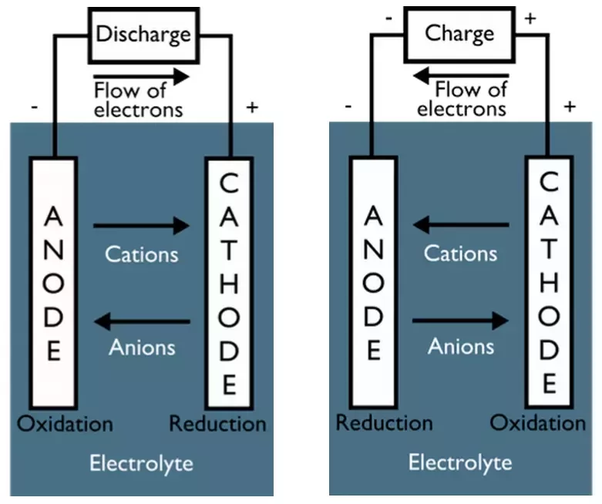
Электрический аккумулятор является классическим примером возобновляемого химического источника электрического тока. Он может быть в двух режимах – зарядки и разрядки. Направление электрического тока в этих разных случаях будет в самом аккумуляторе прямо противоположным, хотя полярность электродов не меняется. В зависимости от этого назначение электродов будет разным:
- При зарядке — положительный электрод будет принимать электрический ток (Анод), а отрицательный отпускать (Катод).
- При разрядке – наоборот, положительный электрод будет отпускать электрический ток (Катод), а отрицательный принимать (Анод).
- При отсутствии движения электрического тока — разговоры об аноде и катоде бессмысленны.
В электрохимии
Далее, рассмотрим другую отрасль:
В электрохимии пользуются другими определениями, более понятными читателю и специалисту: “анод – это электрод, где протекают окислительные процессы“, а “катод – это электрод, где протекают восстановительные процессы“.
Но в этой терминологии нет места электронным приборам и схемотехнике — поэтому трудно сказать, как тут течёт ток?
Определение:
В химических окислительно-восстановительных реакциях:
- Процесс отдачи электронов частицей — называется «окислением» (при этом: нейтральная частица превращается в положительный ион [металлы], а отрицательный ион — нейтрализуется).
- Процесс принятия электронов частицей — называется «восстановлением» (при этом: положительный ион нейтрализуется [металлы], а нейтральная частица превращается в отрицательный ион).
- Частицы, отдающие электроны, называются «восстановители», они окисляются. Частицы, принимающие электроны, называются «окислителями», они восстанавливаются.
- В химических окислительно-восстановительных реакциях «окисление» и «восстановление» взаимосвязаны (общее число электронов отдаваемых всеми восстановителями равно общему числу электронов, присоединяемых всеми окислителями).
(Здесь: Частица = атом, молекула или ион. Ион = не нейтральная частица.)
Определение:
Заряд иона кратен заряду электрона. Понятия и термины «ион», «катион», «аонион» — также ввёл М.Фарадей (в 1834 году):
- Катионы — положительно заряженные ионы, движущиеся в растворе электролита к отрицательному полюсу (катоду).
- Анионы — отрицательно заряженные ионы, движущиеся в растворе электролита к положительному полюсу (аноду).
Определение:
Электрохимические процессы — это окислительно-восстановительные реакции, которые сопровождаются возникновением электрического тока или вызываются электрическим током. Выделяют две группы электрохимических процессов:
- процессы превращения электрической энергии в химическую (электролиз);
- процессы превращения химической энергии в электрическую (гальванические элементы).
В электрохимических процессах окислительная и восстановительная полуреакции пространственно разделены, а электроны переходят от «восстановителя» к «окислителю» не непосредственно, а по проводнику внешней цепи, создавая электрический ток (здесь наблюдается взаимное превращение химической и электрической форм энергии).
Простейшая электрохимическая система состоит из двух электродов – проводников первого рода с электронной проводимостью, находящихся в контакте с жидким (раствор, расплав) или твердым электролитом — ионным проводником второго рода. Электроды замыкаются металлическим проводником, образующим внешнюю цепь электрохимической системы.
Итак: что есть Катод? что есть Анод?
Данное определение ЗАВИСИТ от причины, инициирующей электрический ток:
* В гальванических элементах — разность потенциалов между электродами (по определению ГОСТ 15596-82: ‘+’ на Катоде, ‘-‘ на Аноде) возникает ВНУТРИ самого элемента, из-за химических процессов между электролитом и электродами (элемент является ГЕНЕРАТОРОМ) — источник энергии во внешней цепи не требуется, электрический ток и так потечёт во внешнюю цепь из элемента (через его катод). 
* А при электролизе/легировании/зарядке аккумулятора, когда происходящие в электролите химические реакции требуют поглощения внешней энергии (элемент является ПОТРЕБИТЕЛЕМ) — требуется внешний источник электрического тока, включённый в разрыв проводника внешней цепи — он будет ИЗВНЕ создавать разность потенциалов между электродами, и ИЗВНЕ вкачивать ток в элемент (через его анод). С этой точки зрения, как для всех потребителей энергии в электрической цепи, как и для обычного диода: электрод, в который входит ток, называется анод — на нём ИЗВНЕ поддерживается больший потенциал ‘+’. А на Катоде, соответственно, ИЗВНЕ поддерживается меньший потенциал ‘-‘.
Хотя тут есть маленькая путаница, требуется важное замечание: по определению электрохимии, и в этом случае, на аноде всё равно будут протекать «окислительные процессы», а на катоде – «восстановительные процессы». Тип химических реакций на Аноде и Катоде остался прежний, хотя анод и катод сменили знаки! Как так?
На самом деле, не Анод и Катод сменили знаки, а это физические электроды, сохранив знаки полярности, сменили роль и название: тот электрод, что в гальваническом источнике испускал ток и назывался Катодом -> теперь называется Анод; а вместо Анода -> Катод. Это потому что теперь электрический ток толкается ИЗВНЕ, причём в обратную сторону — направление тока изменилось, соответственно, и физические электроды сменили название. Например: ‘-‘ электрод, который в гальваническом элементе (при разряде) «окислялся» — в режиме потребителя тока (при заряде) «восстанавливается» — на этом принципе работает зарядка аккумулятора. 
Пример
Пример: Опущенная в электролит для никелирования («восстановления») или для электрохимического полирования («окисления») — деталь может быть и катодом и анодом — в зависимости от того наносится на нее другой слой [положительных ионов] металла или снимается. Требуется внешний источник питания…
Пояснение: при никелировании, на детали-электроде необходимо поддерживать отрицательный заряд, чтобы из раствора электролита на неё притягивались и осаждались («восстанавливались») положительные ионы металла — ток из такого электрода должен выходить во внешнюю цепь (а электроны, соответственно, поступать из внешней цепи) — это катод.
Как определить анод и катод
Классические термины из физики и химии часто встречаются в инструкциях к использованию современных приборов. Необходимо точно знать, что такое определение под собой подразумевает и как его применять к тем или иным конструкциям и явлениям.
- Что такое анод и катод
- Анод
- Катод
- Как определить анод и катод
- Сфера применения
- Электрохимия
- Гальванотехника
- Вакуумные и полупроводниковые электроприборы
Что такое анод и катод
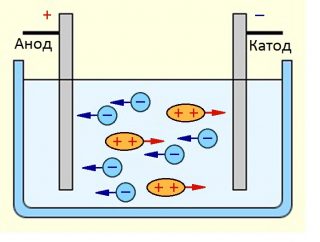
Потребитель сталкивается с понятиями анод и катод при зарядке и разрядке аккумулятора, зарядке и обслуживании батареи.
Понять разницу между катодом, анодом, положительным и отрицательным зарядом проще всего, вспомнив некоторые положения из электрохимии.
- Гальванические элементы – электрический ток производится благодаря текущей химической реакции. Именно на этом принципе работают батарейки и аккумуляторы. Поэтому их называют химическими источниками тока.
- Электролиз – химическая реакция, которая протекает за счет включения в систему источника электроэнергии.
В обоих случаях один из электродов несет более высокий потенциал. Этот электрод считается положительным. Электрод с более низким потенциалом и необязательно отрицательным, будет носить название отрицательный. Ток, соответственно, течет от носителя более высокого потенциала к носителю более низкого потенциала.
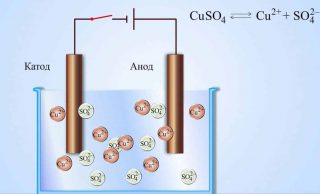
По определению анодом выступает электрод, на котором протекает окислительная реакция. Это означает, что электрод служит источником электронов. В химии его же нередко именуют восстановителем.
Катод
Под катодом подразумевают электрод, на котором протекает реакция восстановления. Здесь электрод забирает электроны и называется окислителем.
Принимая, что ток является движением положительно заряженных частиц, а не отрицательных, получается, что ток в растворе идет от катода к аноду. В цепи, соединяющей элементы гальванической пары, электроны идут от минуса к плюсу и с этой точки зрения катод является плюсом, а анод – минусом.
Противоречие кажущееся, ведь направление тока определяется движением положительных частиц, хотя фактически в металлической цепи его обеспечивает движение электронов.
Как определить анод и катод
Если с батарейкой все довольно просто (полюс и минус не меняются местами), то с зарядкой аккумулятора дело обстоит сложнее.
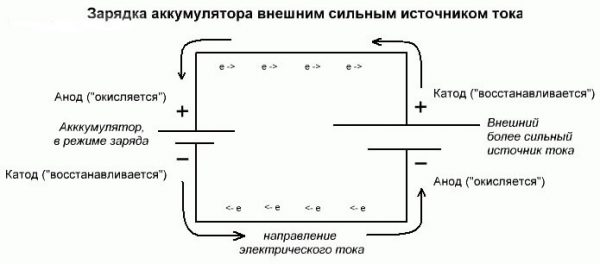
Во время зарядки разность между большим и меньшим потенциалом увеличивается, то есть потенциал положительного электрода становится выше, чем его же потенциал в покое – накапливается заряд, а потенциал отрицательного электрода становится меньше, чем он же в состоянии покоя. Отсюда вытекает, что положительный электрод выступает анодом, а отрицательный – катодом.
При использовании устройства потенциал положительного электрода (анода) всегда остается больше, чем потенциал отрицательного (катода). Но во время цикла разрядки/зарядки роль электрода меняется: при разрядке положительным становится катод, отрицательным – анод. Во время зарядки положительным выступает анод, отрицательным – катод.
Если речь идет о растворах и электрофизических реакциях в них, проще запомнить, что катионы – всегда частицы с положительным зарядом, а значит двигаются к минусу. Анионы – частицы всегда с отрицательным зарядом и двигаются к плюсу.
Что такое анод и катод, в чем их практическое применение
Анод и катод известны многим людям, даже тем, которые не связаны с электрикой или электроникой. Катод это электрод, имеющий отрицательный заряд, а анод заряжен положительно. Чтобы это легко и быстро запомнить, есть одно правило. В слове «катод» пять букв, также как и в слове «минус», а «анод» – четыре буквы, аналогично слову «плюс». Катоды и аноды используются для электролиза, в том числе для получения многих металлов, например алюминия. Они нашли широкое применения в современной промышленности, электроники и других сферах.
В статье будет подробно рассказано о том, что такое Анод и катод, а также для чего именно они нужны и какие физические законы за ними стоят. В качестве дополнения, настоящая статья имеет два ролика и статью, которую можно скачать по ссылке.

Процессы, протекающие при электролизе
Электролиз получил широкое распространение в металлургии цветных металлов и в ряде химических производств. Такие металлы, как алюминий, цинк, магний, получают главным образом путем электролиза. Кроме того, электролиз используется для рафинирования (очистки) меди, никеля, свинца, а также для получения водорода, кислорода, хлора и ряда других химических веществ.
Сущность электролиза заключается в выделении из электролита при протекании через электролитическую ванну постоянного тока частиц вещества и осаждении их на погруженных в ванну электродах (электроэкстракция) или в переносе веществ с одного электрода через электролит на другой (электролитическое рафинирование). В обоих случаях цель процессов – получение возможно более чистых незагрязненных примесями веществ.
Любой электровакуумный прибор имеет электрод, предназначенный для испускания (эмиссии) электронов. Этот электрод называется катодом. Электрод, предназначенный для приема эмиттированных катодом электронов, называется анодом. На анод подают более высокий и положительный относительно катода потенциал.
В отличие от электронной электропроводности металлов в электролитах (растворах солей, кислот и оснований в воде и в некоторых других растворителях, а также в расплавленных соединениях) наблюдается ионная электропроводность. Электролиты являются проводниками второго рода. В этих растворах и расплавах имеет место электролитическая диссоциация – распад на положительно и отрицательно заряженные ионы.
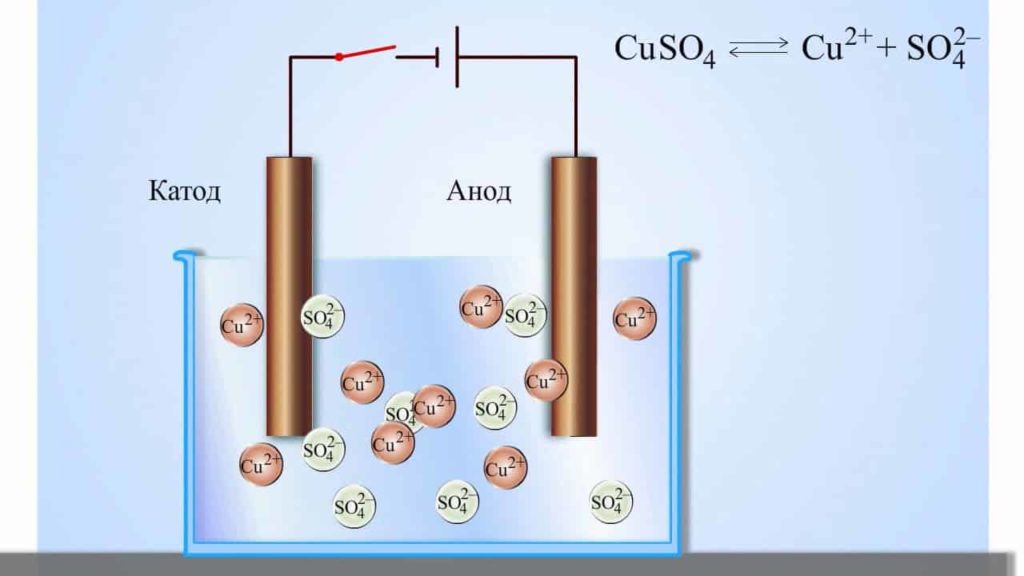
Если в сосуд с электролитом – электролизер поместить электроды, присоединенные к электрическому источнику энергии, то в нем начнет протекать ионный ток, причем положительно заряженные ионы – катионы будут двигаться к катоду (это в основном металлы и водород), а отрицательно заряженные ионы – анионы (хлор, кислород) – к аноду. У анода анионы отдают свой заряд и превращаются в нейтральные частицы, оседающие на электроде. У катода катионы отбирают электроны у электрода и также нейтрализуются, оседая на нем, причем выделяющиеся на электродах газы в виде пузырьков поднимаются кверху.
Электрический ток во внешней цепи представляет собой движение электронов от анода к катоду. При этом раствор обедняется, и для поддержания непрерывности процесса электролиза приходится его обогащать. Так осуществляют извлечение тех или иных веществ из электролита (электроэкстракцию). Если же анод может растворяться в электролите по мере обеднения последнего, то частицы его, растворяясь в электролите, приобретают положительный заряд и направляются к катоду, на котором осаждаются, тем самым осуществляется перенос материала с анода на катод. Так как при этом процесс ведут так, чтобы содержащиеся в металле анода примеси не переносились на катод, такой процесс называется электролитическим рафинированием.

Такой потенциал называется нормальным потенциалом вещества. Если на электрод подать более отрицательный потенциал, то на нем начнется выделение вещества (катодный процесс), если же более положительный, то начнется его растворение (анодный процесс). Значение нормальных потенциалов зависит от концентрации ионов и температуры. Принято считать нормальный потенциал водорода за нуль. В табл. 1 даны нормальные электродные потенциалы некоторых водных растворов веществ при +25° С.
Если в электролите имеются ионы разных металлов, то первыми на катоде выделяются ионы, имеющие меньший отрицательный нормальный потенциал (медь, серебро, свинец, никель), щелочноземельные металлы выделить труднее всего. Кроме того, в водных растворах всегда имеются ионы водорода, которые будут выделяться ранее, чем все металлы, имеющие отрицательный нормальный потенциал, поэтому при электролизе последних значительная или даже большая часть энергии затрачивается на выделение водорода.
Путем специальных мер можно воспрепятствовать в известных пределах выделению водорода, однако металлы с нормальным потенциалом меньше 1 В (например, магний, алюминий, щелочноземельные металлы) получить электролизом из водного раствора не удается. Их получают разложением расплавленных солей этих металлов. Нормальные электродные потенциалы веществ являются минимальными, при них начинается процесс электролиза, практически требуются большие значения потенциала для развития процесса.
Разность между действительным потенциалом электрода при электролизе и нормальным для него потенциалом называют перенапряжением. Оно увеличивает потери энергии при электролизе. С другой стороны, увеличивая перенапряжение для ионов водорода, можно затруднить его выделение на катоде, что позволяет получить электролизом из водных растворов ряд таких более отрицательных по сравнению с водородом металлов, как свинец, олово, никель, кобальт, хром и даже цинк. Это достигается ведением процесса при повышенных плотностях тока на электродах, а также введением в электролит некоторых веществ.
Течение катодных и анодных реакций при электролизе определяется следующими двумя законами Фарадея.
- Масса вещества mэ, выделившегося при электролизе на катоде или перешедшего с анода в электролит, пропорциональна количеству прошедшего через электролит электричества Iτ: mэ = α/τ,здесь а – электрохимический эквивалент вещества, г/Кл.
- Масса выделенного при электролизе вещества одним и тем же количеством электричества прямо пропорциональна атомной массе вещества А и обратно пропорциональна его валентности n: mэ= А / 96480n, здесь 96480 – число Фарадея, Кл х моль -1 .
Таким образом, электрохимический эквивалент вещества α= А / 96480n представляет собой массу вещества в граммах, выделяемую единицей проходящего через электролитическую ванну количества электричества – кулоном (ампер-секундой).
Для меди А = 63,54, n =2, α =63,54/96480 -2 = 0,000329 г/Кл, для никеля α =0,000304 г/Кл, для цинка α=0,00034 г/Кл. В действительности масса выделившегося вещества всегда меньше указанной, что объясняется рядом побочных процессов, проходящих в ванне (например, выделением водорода на катоде), утечками тока и короткими замыканиями между электродами. Отношение массы фактически выделившегося вещества к массе его, которая должна была бы выделиться по закону Фарадея, носит название выхода вещества по току η1.
Мощность, потребляемая при электролизе, равна: Рэл = IUэл = I(Ер + Еп + Uэ + Uс). Из этой мощности только первая составляющая расходуется на проведение реакций, остальные являются тепловыми потерями процесса. Лишь при электролизе расплавленных солей часть теплоты, выделяющейся в электролите IUэ, используется полезно, так как расходуется на расплавление загружаемых в электролизер солей.
Эффективность работы электролизной ванны, может быть оценена массой вещества в граммах, выделяемого на 1 Дж затраченной электроэнергии. Эта величина носит название выхода вещества по энергии.Ее можно найти по выражению qэ = (αη1)/Uэл100, здесь α – электрохимический эквивалент вещества, г/Кл, η1 – выход по току, Uэл – напряжение на электролизере, В.
Определение анода и катода
Для начала возьмем очень серьезный документ, который является ЗАКОНОМ для науки, техники и, конечно, школы. Это «ГОСТ 15596-82. ИСТОЧНИКИ ТОКА ХИМИЧЕСКИЕ. Термины и определения». Там на странице 3 можно прочесть следующее: «Отрицательный электрод химического источника тока это электрод, который при разряде источника является анодом». То же самое, «Положительный электрод химического источника тока это электрод, который при разряде источника является катодом». (Термины выделены мной. БХ). Но тексты правила и ГОСТа противоречат друг-другу. В чем же дело?
А всё дело в том, что, например, деталь, опущенная в электролит для никелирования или для электрохимического полирования, может быть и анодом и катодом в зависимости от того наносится на нее другой слой металла или, наоборот, снимается. Электрический аккумулятор является классическим примером возобновляемого химического источника электрического тока. Он может быть в двух режимах – зарядки и разрядки. Направление электрического тока в этих разных случаях будет в самом аккумуляторе прямо противоположным, хотя полярность электродов не меняется.

«Поэтому, во избежание неясности и неопределенности, а также ради большей точности, – записал в своих исследованиях М.Фарадей в январе 1834г., – я в дальнейшем предполагаю применять термины, определение которых сейчас дам».
Каковы же причины введения новых терминов в науку Фарадеем? А вот они: «Поверхности, у которых, согласно обычной терминологии, электрический ток входит в вещество и из него выходит, являются весьма важными местами действия и их необходимо отличать от полюсов». В те времена после открытия Т. Зеебеком явления термоэлектричества имела хождение гипотеза о том, что магнетизм Земли обусловлен разностью температур полюсов и экватора, вследствие чего возникают токи вдоль экватора. Она не подтвердилась, но послужила Фарадею в качестве «естественного указателя» при создании новых терминов. Магнетизм Земли имеет такую полярность, как если бы электрический ток шел вдоль экватора по направлению кажущегося движения солнца.
Фарадей записывает: «На основании этого представления мы предлагаем назвать ту поверхность, которая направлена на восток – анодом, а ту, которая направлена на запад – катодом». В основе новых терминов лежал древнегреческий язык и в переводе они значили: анод – путь (солнца) вверх, катод – путь (солнца) вниз.
В русском языке есть прекрасные термины ВОСХОД и ЗАХОД, которые легко применить для данного случая, но почему-то переводчики Фарадея этого не сделали. Мы же рекомендуем пользоваться ими, ибо в них корнем слова является ХОД и, во всяком случае, это напомнит пользователю термина, что без движения тока термин не применим. Для желающего проверить рассуждения создателя термина с помощью других правил, например правила пробочника, сообщаем, что северный магнитный полюс Земли лежит в Антарктиде, возле Южного географического полюса.
Ошибкам в применениях терминов АНОД и КАТОД нет числа. В том числе и в зарубежных справочниках и энциклопедиях. Поэтому в электрохимии пользуются другими определениями, более понятными читателю. У них анод – это электрод, где протекают окислительные процессы, а катод – это электрод, где протекают восстановительные процессы. В этой терминологии нет места электронным приборам, но при электротехнической терминологии указать анод радиолампы, например, легко. В него входит электрический ток. (Не путать с направлением электронов).
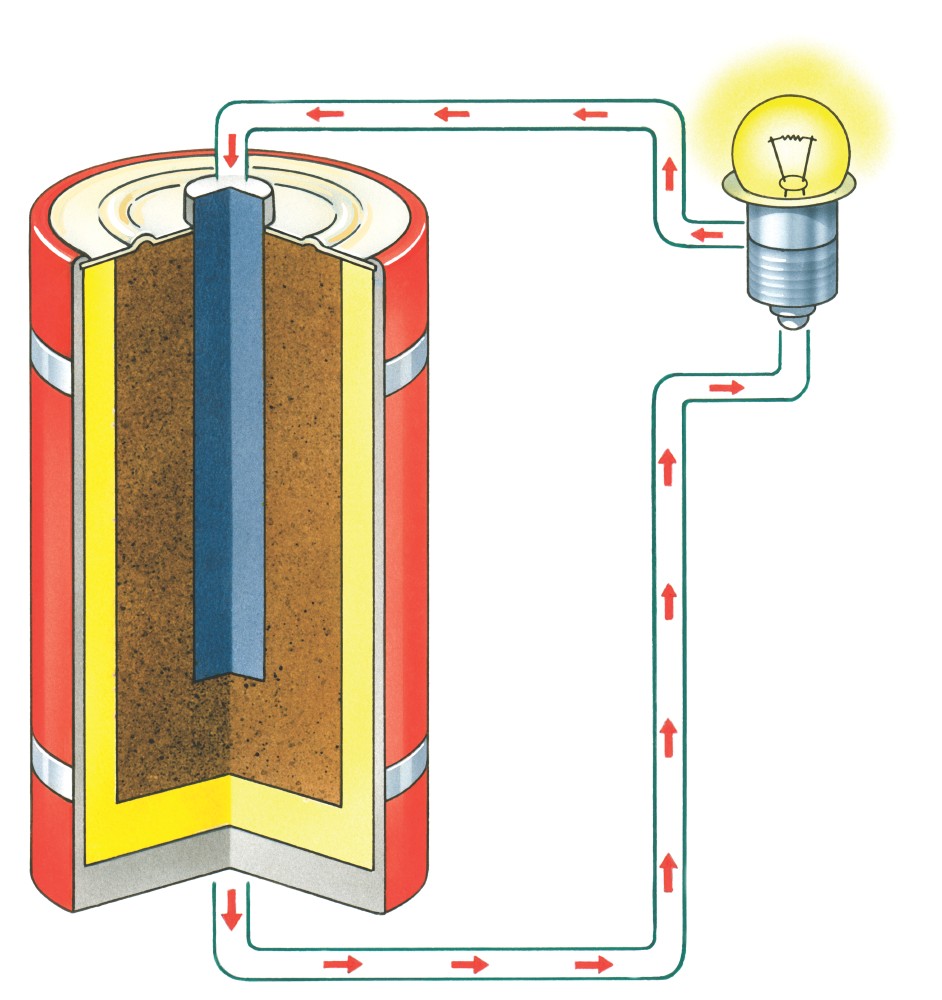
Основные свойства катодов
Любой электровакуумный прибор имеет электрод, предназначенный для испускания (эмиссии) электронов. Этот электрод называется катодом. Электрод, предназначенный для приема эмиттированных катодом электронов, называется анодом. На анод подают более высокий и положительный относительно катода потенциал. Катод должен отдавать с единицы поверхности большой ток эмиссии при возможно низкой температуре нагрева и обладать большим сроком службы. Нагрев катода в электровакуумном приборе производится протекающим по нему током.
Такие термоэлектронные катоды разделяются на две основные группы:
- катоды прямого накала,
- катоды косвенного накала (подогревные).
Катоды прямого накала представляют собой металлическую нить, которая непосредственно разогревается током накала и служит для излучения электронов.Поверхность излучения катодов прямого накала невелика, поэтому от них нельзя получить большой ток эмиссии. Малая теплоемкость нити не позволяет использовать для нагрева переменный ток. Кроме того, при нагреве переменным током температура катода не постоянна во времени, а следовательно, меняется во времени и ток эмиссии.
Положительным свойством катода прямого накала является его экономичность, которая достигается благодаря малому количеству тепла, излучаемого в окружающую среду вследствие малой поверхности катода. Катоды прямого накала изготовляются из вольфрамовой и никелевой проволоки. Однако большая работа выхода (W = 4,2÷4,5 в) определяет высокую рабочую температуру катода, вследствие чего катод становится неэкономичным. Для повышения экономичности катода вольфрамовую или никелевую проволоку (керн) «активируют» — покрывают пленкой другого элемента. Такие катоды называются активированными.

Работа выхода катода с такой мономолекулярной электроположительной пленкой оказывается меньше работы выхода электрона как из основного металла, так и из металла пленки. При покрытии керна электроотрицательной пленкой, например кислородом, работа выхода катода увеличивается. Подогревные катоды выполняются в виде никелевых гильз, поверхность которых покрывается активным слоем металла, имеющим малую работу выхода. Внутри катода помещается подогреватель— вольфрамовая нить или спираль, подогрев которой может осуществляться как постоянным, так и переменным
Для изоляции подогревателя от гильзы внутренность последней покрывается алундом (Аl2O3). Подогревные катоды, благодаря их большой тепловой инерции, обычно питают переменным током, значительная поверхность гильзы обеспечивает большой эмиссионный ток. Подогревные катоды, однако, менее экономичны и разогреваются значительно дольше, чем катоды прямого накала.
Катод и анод
Иногда требуется подключить к источнику питания постоянного тока электроды какого-либо прибора или элемента. Их присоединяют, соблюдая полярность. Катод и анод – так называются проводники (электроды) устройства, с помощью которых выполняется это подключение. Однозначного понятия этих двух терминов нет. Их различают в зависимости от того, в каких химических и физических процессах применяют эти обозначения.

Понятие катода и анода
В электрической технике вывод, присоединяемый к положительной клемме источника питания (ИП), называют анодом (А). Электрод, присоединённый к минсовому выводу ИП, – катодом (К). В переводе с греческого языка анод – «восхождение, движение вверх», катод – «нисхождение, движение вниз». С этими названиями можно встретиться в таких разделах физики и химии, как:
- гальванические источники питания;
- электролиз и гальванотехника;
- полупроводники и вакуумная электроника.
Кроме того, этими терминами обозначаются выводы элементов на схемах и знаки их заряда.
Обозначение в электрохимии и цветной металлургии
Понятие анодов в электролитических процессах применимо в отношении положительно заряженных электродов. Электролиз, с помощью которого выделяются или очищаются различные химические элементы, – это влияние электрического тока на электролит. Электролитом выступают растворы солей или кислот. Другим электродом, участвующим в этой реакции, выступает катод.
Внимание! На отрицательно заряженном катоде (К) осуществляется реакция восстановления, на аноде (А) – процесс окисления. При этом «А» может частично разрушаться, участвуя в очищении металлов от нежелательных добавок.
В металлургической промышленности аноды используют при нанесении защитных слоёв на продукт электрохимическим методом (гальваника) или электро-рафинированием. Электрическое очищение позволяет растворять на «А» черновой металл (с примесями) и осаждать его на «К» уже в очищенном виде.
Ряд часто применяемых анодов – изготовленные из металлов:
- цинка;
- меди;
- никеля;
- кадмия;
- свинцовые (сплав свинца с сурьмой);
- серебра;
- золота;
- платины.
Никелирование, оцинкование и прочее нанесение защитных или эстетически востребованных покрытий на изделия выполняются в основном из недрагоценных металлов.
С помощью «А» из драгметаллов повышают электропроводность компонентов электрических изделий и наносят слои благородных металлов на ювелирные украшения.
К сведению. Осаждаемый на катоде чистый металл также называют «катодом». Например, чистая медь полученная таким образом именуется «медный катод». Дальше её используют для изготовления медной фольги, проволоки и прочего.

Анод и катод в вакуумных электронных приборах
Электронная лампа является простейшим вакуумным устройством. Она состоит из следующих деталей:
- катода;
- сетки;
- анода.
Три этих элемента составляют вакуумный диод. У него «К» цилиндрической формы, внутри которого располагается нить накаливания. Она подогревает «К» для увеличения термоэлектронной эмиссии. В таких приборах электроны покидают «К» и в вакууме направляются к «А», тем самым создавая электрический ток. Анод – это электрод лампы с положительным потенциалом. Он выполняется в виде короба окружающего сетку и «К». Может быть из молибдена, тантала, графита, никеля. Его конструкция различна, порой имеет рёбра для теплоотвода.
Сетка – элемент, расположенный посередине, управляет потоком частиц. Чаще всего она выполнена в виде спирали, обвивающей катод.
Важно! Чем больше площадь поверхности катода, и чем сильнее он разогрет, тем больший ток протекает через лампу.

Анод и катод у полупроводниковых приборов
Полупроводниковые элементы проводят электричество в определённом направлении. Если рассматривать полупроводниковый диод, то его электроды также носят название «катод» и «анод». При прикладывании к нему прямого напряжения: положительный заряд к аноду, диод открыт. Если положительный потенциал приходит на катод, диод закрыт. Такой диод имеет p-n переход между двумя этими областями и требователен к приложенной полярности. Вывод элемента из p-области именуется «А», из n-области – «К».

Знак анода и катода
Каким знаком обозначается «К», каким «А», зависит от того, какая процедура и в какой области рассматривается. В электрохимии есть два устройства, имеющие различие в обозначении знаками: электролизёр и гальванический элемент.
При электролизе (окислительно-восстановительном химическом взаимодействии под влиянием внешнего ИП) минусом «-» обозначают катод. Именно на нём восстанавливаются металлы, из-за избытка электронов. Плюсом «+», в свою очередь, маркируют анод (положительный электрод), где металлы окисляются из-за недостатка отрицательно заряженных частиц.

В гальваническом элементе окисление происходит без внешнего воздействия электричества. Если взять в качестве примера медно-цинковую батарею, то большое количество электронов (минус) скапливается на аноде. Они при продвижении по внешней цепи участвуют в восстановлении меди. Значит, в этом случае положительным электродом будет катод.
Внимание! У гальванических элементов плюсом является катод, минусом – анод. У электролизёров наоборот – плюсом считают анод, минусом – катод.

У полупроводниковых приборов, как знак, так и термин, чётко закреплены за выводами детали. Анод – это «плюс», катод – это «минус» диода.
Почему существует путаница
Всё происходит от того, что нет чёткой привязки минуса и плюса к компонентам, которые называются «К» и «А». Ещё Майкл Фарадей придумал простое правило маркировки полярности для этой пары электродов. Что такое анод, по его объяснениям? Учёный при запоминании определения предлагал проводить аналогию с Солнцем. Куда ток входит (восход) – это анод, куда ток выходит (закат) – это катод. У аккумуляторов полярность на аноде и катоде изменяется от того, работает он как гальванический элемент (при разряде) или как электролизёр (при заряде).
Сварка постоянным током также неоднозначно определяет «А» и «К» при зажигании дуги прямой или обратной полярностью.

Как определить анод и катод
Что это такое катод и анод, выясняют в частных моментах: при определении выводов у полупроводниковых элементов или при идентификации электродов в электрохимических процессах.
Полупроводниковый диод требует позиционного размещения в электросхемах. Для правильного соединения необходимо отождествить выводы. Это можно сделать по следующим признакам:
- маркировка, нанесённая на корпус элемента;
- длина выводов детали;
- показания тестера при измерениях в режиме омметра или проверки диодов;
- использование источника тока с известной полярностью.
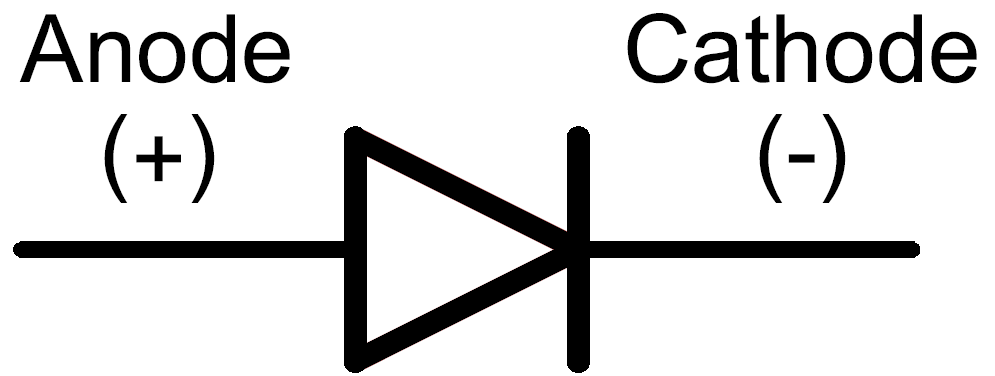
Маркировка полупроводников такого типа может быть выполнена при помощи нанесения на корпус графического обозначения диода. Тогда минус (К) – это вывод со стороны вертикальной линии, в которую упирается контур стрелки. Ножка диода, от которой выходит стрелка, – это плюс (А). Так графически указано прямое направление тока – от «А» к «К».
Другим способом обозначения анода у диодного элемента могут быть нанесённые на корпус одна или две цветные точки или пара узких колец. Существуют конструктивно выполненные диоды, у которых минусовой (катодный) вывод обозначен широким серебряным кольцом. Диод 2А546А-5 (ДМ) служит таким примером.

Длина ножек светодиодов, ни разу не паянных в платы, также может указывать на полярность выводов. У led-диодов длинная ножка – это положительный электрод, короткая – отрицательный вывод. К тому же форма корпуса (обрез края окружности) может служить ориентиром.

При определении мультиметром полярности контактных выводов полупроводника подключают его в режиме тестирования диодов. Если на дисплее появились цифры, значит, диод подключён в прямом направлении. При этом красный щуп подсоединён к аноду «+», чёрный – к катоду «-».
Если под рукой нет тестера, определить названия выводов диода можно, собрав последовательную цепь из батарейки, лампочки и диода. При прямом включении лампочка загорится, значит, плюс батарейки – на аноде и аналогично минус – на другом электроде.
Информация. Электроды светодиода можно идентифицировать с помощью постоянного ИП с заведомо известной полярностью и включенного последовательно резистора, ограничивающего ток. Свечение элемента укажет на прямое включение. Для этой цели можно взять батарейку RG2032 на 3 вольта и резистор сопротивлением 1кОм.

Что касается полупроводников, всегда существует строгое соответствие наименований. В других случаях правильное определение проходящих электрохимических реакций поможет чётко ориентироваться в отождествлении электродов.
Видео
Бактерии для септика и выгребной ямы

Немного теории

Выгребные ямы связаны с множеством неудобств (мухи, неприятный аромат и это лишь начало). Плюс они регулярно наполняются, нуждаясь в последующей очистке. В итоге вызывают ассенизаторскую машину. Забот мало: установил шланг для высасывания отходов из ямы, после чего убрал его по окончанию процедуры. Но во время очистки запахи успевают «порадовать» как собственника дома, так и множество соседей. Кроме этого за помощь ассенизатора надо платить, а если семья большая, то пользоваться услугами и тратить деньги приходится регулярно.
Кроме откачки нужна дезинфекция санузла. Чаще всего применяют хлорку. Но использование указанного средства вредит экологии. Так, к примеру, восстановление химически обработанного грунта занимает много времени. Плюс ко всему хлор разъедает очистные сооружения. В итоге собственник вынужден менять либо переустанавливать туалет. На нас хлор тоже влияет негативно. К примеру, это вещество разъедает кожный покров и пр.
Рассмотренные проблемы решают бактерии. Представленные вещества безвредны для экологии, а также уничтожают вредоносных микробов.
Об особенностях и принципе работы

Производители искусственно растят микроорганизмы, помогающие утилизировать стоки. Это живые бактерии, существующие и в натуральных условиях, однако в значительно меньшем содержании. Микробы, предназначенные для очистных сооружений, безопасны для человека и экологической обстановки. Для жизни подобным «помощникам» нужно питание, в виде которого могут использоваться органические остатки. К примеру, бактерии питаются и утилизируют кал, остатки еды и т.д. Искусственные материалы (пластиковые кучки, металлические изделия и т.д.) микроорганизмы, к сожалению, не утилизируют. Они расщепляют органические отходы преимущественно на воду, а также углекислоту.
Иногда выпадает незначительный объем натурального осадка. В итоге углекислота испаряется, очищенная вода уходит в грунт либо сливается. На дне формируется минеральный осадок, применяемый в виде удобрения. Обращаем внимание, что при недостаточном объеме питания микроорганизмы для очистки стоков погибают.
Перед приобретением препарата, необходимо понимать принцип функционирований бактерий для септиков. Биопрепараты функционируют идентичным образом. В упаковке имеется колония микроорганизмов, которые «спят». Для «пробуждения» надо сделать раствор по установленной формуле. Для средств предусмотрен уникальный рецепт, поскольку везде используются различные микроорганизмы. Чаще всего на основании накопленного опыта можем сказать, что сухие препараты разводятся в жидкости, иногда надо добавить для соблюдения рецепта органику.
Жидкие препараты выливаются в очистное сооружение либо разводятся согласно предоставленному рецепту. Чаще всего до полного «пробуждения» проходит некоторое время. Затем раствор нужно сливать в канализацию. Спустя несколько часов станет заметным эффект: упадет уровень стоков и уйдет неприятный аромат. Не беспокойтесь, если на поверхности возникнут пузыри. Таким образом формируется и уходит углекислота.
Какие существуют виды биобактерий?

- Аэробы – требуют для существования кислород.
- Анаэробы – требуют для существования нитраты, а также углекислоту. Кислород не нужен.
В быту преимущественно применяют анаэробные бактерии либо комплекс из двух видов микроорганизмов. На промышленных объектах чаще всего выбирают средства, содержащие оба типа бактерий.
Если в препарате имеются и аэробы, и анаэробы, то это биоактиватор. В подобных случаях к средствам добавляют ферменты, ускоряющие расщепление стоков и улучшающие эффективность функционирования бактерий.
Анаэробные и аэробные микроорганизмы (бактерии): в чем их различие?
Читайте в статье.
Бактерии живут во всем окружающем нас мире, в земле, воздухе, на вашем рабочем столе и экране телефона. Основная классификация бактерий основана на том, необходим ли им кислород для жизнедеятельности или нет.
Анаэробные бактерии
Анаэробные бактерии не нуждаются в кислороде и способны жить в различных средах, где нет света и кислорода, например, в почве, в желудочно-кишечном тракте животных и человека и т.д. Анаэробные бактерии отвечают за гниение, процессе их деятельности органические соединения постепенно разлагаются с выделением метана, который и является причиной неприятного гнилостного запаха.
Анаэробные бактерии царствуют в пластиковых септиках
Пластиковые септики представляют собой емкость с небольшими отверстиями, иногда разделенную перегородками. Малое количество кислорода дает плодородную среду для появления и развития этих бактерий. Отходы в таком септике не перерабатываются полностью – часть из них образуют твердый осадок, оседая на дно и медленно перегнивая. Степень очистки стоков в таком септике не превышает 30-40%, а темная, влажная среда способствует развитию вредных микроорганизмов, в связи с чем, воду и отходы с такого септика нельзя использовать для удобрения – это может привести к заражению. С небольшой периодичностью такие септики необходимо откачивать ассенизаторской машиной.
Наглядный пример принципа работы такого септика – обычный деревянный туалет, имеющий характерный запах работы анаэробных организмов.
Именно анаэробные микроорганизмы вызывают воспалительно-гнойные заболевания различных видов:
- гангрены;
- абсцессы;
- пневманию;
- менингиты;
- инфекции глубоких тканей;
- некрозы и другие заболевания инфекционного характера.
Однако другой подвид анаэробных бактерий также являются частью нормальной микрофлоры кишечника человека и полости рта. Таким образом, различные подвиды анаэробов могут быть как полезными, так и опасными для человека.
Аэробные бактерии
Другой группой бактерий выступают аэробные микроорганизмы. Они живут только в присутствии кислорода и вызывают не гниение, а окисление органики в процессе синтеза энергии, при этом выделяется тепло и углекислота, а не метан, поэтому неприятного запаха в процессе переработки отходов жизнедеятельности человека не возникает. Органические отходы под действием аэробов преобразуются в активный ил и чистую, прозрачную воду. Именно на этом принципе работает любая автономная канализация для загородного дома: как чешский Топас, так и его русский аналог – Юнилос Астра, и недавно появившиеся станции Евробион и Биодека.
С помощью постоянной подачи кислорода и поступления органических отходов в станцию биологической очистки, поддерживается существование колонии аэробных бактерий. После переработки сточных вод, чистая вода из автономной канализации удаляется в канаву или дренажный колодец, а активный ил оседает на дне и стенках станции. Активный ил достаточно чистить раз в 3-6 месяцев, в зависимости от активности эксплуатации. Сточные воды очищаются до 98% и чистая вода из станции может использоваться для полива не плодовых деревьев, газонов, мытья дорожек, веранды или машины.
Как попадают бактерии в автономную канализацию
Бактерии в автономной канализации появляются естественным образом после начала ее использования, дополнительное добавление бактерий в нее не требуется. При грамотной установке и эксплуатации согласно рекомендациям производителя, в дальнейшем покупка бактерий также является лишней тратой денег. Первым признаком неправильной работы станции является сильный гнилостный запах из нее, если его нет, то бактерии в вашей станции отлично справляются со своей задачей. В случае появления неприятного запаха из канализации, обратитесь в компанию, которая производила установку станции, возможно, дело вовсе не в гибели бактерий, а в поломке какой-либо системы.
Аэробная и анаэробная среда
При выполнении гематологических исследований используются два типа организмов аэробные и анаэробные. Они отличаются потребностью в наличии кислорода в окружающей среде. Аэробные микроорганизмы могут функционировать только при наличии кислорода, в то время, как анаэробные в нем совсем не нуждаются.
Классификация этих видов проводится на основе реакции на наличие или отсутствие кислорода. Из-за этого аэробные и анаэробные микроорганизмы по-разному выполняют свои функции в процессе клеточного дыхания.
Особенности аэробных микроорганизмов
Аэробные микроорганизмы не могут существовать без кислорода. Он необходим им для роста, развития и участвует в процессах размножения. Благодаря кислороду они способны окислять моносахариды, например, глюкозу.
Генерация энергии в этих микроорганизмах происходит при гликолизе. После него следует цикл Кребса и цепь переноса электронов. Среды, насыщенные кислородом – отличная питательная среда для таких микроорганизмов. Примеры аэробов – бациллы и нокардии.
Типы аэробов
Аэробные микроорганизмы классифицируют по уровню необходимого для жизнедеятельности кислорода:
- Облигатные аэробы или аэрофилы. В обязательном порядке нуждаются в кислороде. Они используют его для клеточного дыхания и окисления органических веществ – сахаров и жиров, из которых получают энергию. Примеры облигатных аэробных микроорганизмов – Nocardia, Mycobacterium tuberculosis и Vibrio cholerae.
- Микроаэрофильные аэробы. Обладают способностью выживать при малых концентрациях кислорода (около 10 процентов). Пример – Хеликобактер пилори.
Бактерии, нуждающиеся в кислороде для выживания, легко выделяются при культивировании в жидкой среде. Так для полноценной жизнедеятельности им необходим кислород, то чтобы выжить они всплывают на поверхность.

Особенности анаэробов
В процессе энергетического обмена эти микроорганизмы не используют кислород. Для этого им необходимы марганец, сера, кобальт, азот, метал или железо. В процессе образования энергии анаэробные микроорганизмы подвергаются ферментации. Для выживания они используют энергию, производимую при анаэробных процессах брожения:
- Молочной кислоты;
- Этанола.
Классификация анаэробных микроорганизмов также определяется по уровню токсичности кислорода:
- Аэротолерантные. Для выживания кислород им не требуется, а его присутствие не наносит им вреда. Пример – лактобациллы.
- Облигатные. Для таких микроорганизмов кислород губителен. Они живут и растут только при полном его отсутствии в среде. Пример – клостридии, метаносарцины.
- Факультативные. На их развитие и жизнедеятельность не влияет наличие кислорода. Они могут жить как при его наличии, так и при отсутствии. Пример – кишечная палочка.
Анаэробы не способны выживать в среде, богатой кислородом. Для облигатных разновидностей он токсичен, а вот факультативным видам он не вредит.
Сходства между аэробами и анаэробами
- Являются прокариотическими микроорганизмами.
- Их начальная стадия клеточного дыхания – гликолиз.
- Их основу составляют патогенные болезнетворные микроорганизмы.
- Применяются в различных сферах промышленности.
Различия аэробов и анаэробов
Отличительные особенности микроорганизмов представлены в таблице.
| Параметр сравнения | Аэробы | Анаэробы |
| Условия выживания | Нуждаются в кислороде, так как он конечный акцептор электронов в их клеточном дыхании | Для клеточного дыхания им не нужен кислород |
| Конечные электронные акцепторы | Кислород | Сера, метан, азот, железо |
| Процессы, участвующие в клеточном дыхании | Гликолиз, Цикл Кребса, Цепь переноса электронов | Гликолиз, Ферментация |
| Разновидности | Облигатные, Микроаэрофильные, Факультативные, Аэротолерантные | Облигатные, Факультативные |
| Среда для роста | Богатые уровнем кислорода среды | Среды, в которых отсутствует кислород |
| Токсичность кислорода | Нетоксичен | Токсичен |
| Кислородные детоксифицирующие ферменты | Присутствуют | Отсутствуют |
| Уровень производства энергии | Высокая эффективность производства энергии | Низкая эффективность производства энергии |
| Примеры | Сенная палочка (Bacillus spp), Синегнойная палочка (Pseudomonas aeruginosa), Палочка Коха (Mycobacterium tuberculosis) | Актиномицеты (Actinomyces), Бактероиды (Bacteroides), Пропионовокислые бактерии (Propionibacterium), Вейлонелла (Veillonella), Пептострепококки (Peptostreptococcus), Порфиромонас (Porphyromonas), Клостридии (Clostridium spp) |
Аэробы и анаэробы требуют различных по уровню кислорода питательных сред для выживания. Аэробным микроорганизмам кислород необходим для энергетического обмена, а анаэробные микроорганизмы его не используют. Вместо этого они используют нитраты, серу и метан. Именно поэтому ключевыми отличиями этих микроорганизмов являются типы конечных акцепторов электронов, которые используются в процессе клеточного дыхания.